
Les Biophysiciens découvrent que les ‘câbles d’eau’ sont des canaux d’information biologiques.
Article traduit à partir d’ Evolution News @DiscoveryCSC du 22 juillet 2020, et complété par des explications et des éclaircissements.
L’eau conduit l’électricité ; elle peut aussi conduire l’énergie et l’information. Les biophysiciens découvrent que les ‘câbles’ constitués d’eau au niveau nanométrique ajustent les actions enzymatiques – et peuvent être en fait indispensables à leur fonctionnement.
Dans une publication d’avril, Evolution News a partagé un fait remarquable concernant la dynéine, une des structures moléculaires qui fonctionnent avec des microtubules.
https://evolutionnews.org/2020/04/journal-prints-intelligent-design-but/
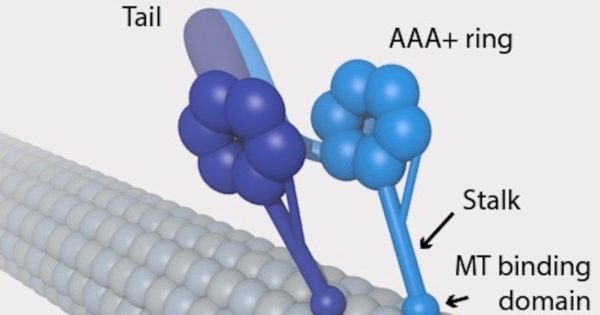
Les scientifiques dans cette histoire émettent la théorie que les molécules d’eau se relient au tube (microtubule) et aide à transmettre de l’énergie kinésique grâce à des ‘vagues/ondes d’eau’ à partir de la réaction du centre cellulaire, où l’ATP est dépensée, vers les ‘pieds’ où la marche à lieu.
L’ATP (adénosine-triphosphate) est une molécule riche en énergie qui libère son énergie en se convertissant en ADP (adénosine-diphosphate). L’ATP est le ‘fuel’ cellulaire. L’ATP est la molécule clef de l’énergétique cellulaire mais elle joue aussi d’autres rôles au sein de la cellule. L’ATP est un nucléotide, c’est-à-dire une molécule formée par un sucre à 5 atomes de carbone, le désoxyribose, une base azotée, l’adénine, et une chaîne de trois acides phosphoriques.Si la molécule d’ATP est trouvée à l’état libre dans les cellules, elle sert également de matériau de construction pour la synthèse des acides nucléiques, la classe de macromolécules essentiellement en charge de l’information génétique. Une cellule possède très peu d’ATP. Et comme elle en consomme en permamence, elle doit constamment en fabriquer (synthétiser) et c’est notamment la respiration cellulaire qui fournit l’énergie nécessaire pour la fabrication de l’ATP en permettant une phosphorylation (addition d’un phosphate à l’ADP).
Ainsi, les molécules d’eau sont positionnées d’une certaine manière afin de créer un tsunami virtuel d’énergie d’un côté à l’autre du système, ce qui entraine le mouvement du pied. Cela demande évidemment une coopération très précise entre les molécules d’eau et les acides aminés contenus dans le tube, le microtubule. Maintenant, d’autres occurrences émergent concernant les systèmes biologiques incorporant des molécules d’eau dans leur spécificité fonctionnelle.
Comment les câbles d’eau fonctionnent-ils ?
Les biophysiciens ont longtemps suspecté que les molécules d’eau facilitent le passage des substrats à travers les canaux des membranes. La mission des canaux des membranes est de permettre à certaines molécules de traverser la membrane cellulaire tout en interdisant l’accès à d’autres. Cela est appelé le transport actif, parce que normalement, les molécules se meuvent par diffusion (transport passif). Les cellules ont besoin d’à la fois attirer les bonnes molécules qui passeront à travers le canal et aussi de les authentifier à travers des ‘filtres de sélectivité’. Et l’eau peut faciliter ce processus via l’électricité. Puisque H2O est bipolaire, les molécules d’eau simples formant une chaine, tenues ensemble par les liens d’hydrogène, deviennent une sorte de ‘câble’ au travers duquel les ions passent. De plus, le fait que des acides aminés soient hydrophiles permet aux canaux biologiques d’attirer les molécules d’eau dans la position exacte à l’intérieur du canal et où elle peut faciliter le filtre de sélectivité.
Un composé hydrophile (du grec ὕδωρ (hydro) « eau », et φιλέω (phileo) « aimer ») est un composé ayant une affinité pour l’eau et tendance à s’y dissoudre. Il est également ionique.
Il peut être soluble dans l’eau (hydrosoluble) ou les solvants polaires. La cellulose (coton), très hydrophile, est insoluble dans la plupart des solvants du fait de sa forte cohésion. Le savon, amphiphile, se dissout à la fois dans l’eau et l’huile, ce qui explique son pouvoir détergent.
Un composé hydrophile est typiquement polaire. Cela lui permet de créer des liaisons hydrogène avec l’eau ou un solvant polaire. Il renferme au moins un groupe fonctionnel tel une amine, un alcool ou une cétone.
Certaines molécules hydrophiles ne se dissolvent pas ; elles peuvent former un colloïde.
Construire des câbles d’eau par design
En 2009, des scientifiques en Inde ont construit un ‘nanotube de peptide’ artificiel juste assez large pour tenir une chaine de molécule d’eau. Chemistry World explique comment achever cela en pratique était plus compliqué qu’en théorie :
L’eau se comporte différemment au niveau nanométrique, en formant des arrangements en file indienne connus en tant que ‘câble d’eau’. Ceux-ci sont importants en biologie parce qu’ils transportent les protons à travers les membranes cellulaires, ce qui est une étape cruciale dans la manière dont la plupart des organismes produisent de l’énergie.
Le mécanisme derrière ce transfert de proton est la chaine classique Grotthuss, où le lien d’Hydrogène laisse les protons bondir entre les molécules d’eau très rapidement. Mais prédire comment ce mécanisme affecte des molécules en file indienne a été un défi. A présent, une équipe menée par Padmanabhan Balaram à l’Indian Institute of Science à Bangalore se penche sur la manière dont les molécules sont configurées, fournissant un modèle utile pour des études futures.
L’expérience dans cet essai initial n’attirait pas l’eau sur les bords du canal mais a démontré la possibilité de le faire. E, 2018, les scientifiques de Cornell et Rensselaer ont réalisé des progrès en construisant des câbles d’eau artificiels. Le news from Rensselaer, “Preuve des câbles d’eau animé par un canal d’eau biologique ‘ raconte que les canaux d’eau biologiques appelés aquaporines fournissent l’inspiration pour leurs expériences biomimétiques.
Les Aquaporines sont des protéines qui servent de canal d’eau afin de réguler le flot de l’eau à travers les membranes de la cellule biologique. Elles enlèvent aussi les excès de sel et les impuretés dans le corps, et c’est cet aspect qui a mené à tant d’intérêt ces dernières années sur la façon de mimer, ou copier les processus biologiques de l’aquaporine, pour de possibles systèmes de désalinisation.
Les expérimentateurs ont construit un canal artificiel avec des tubes d’imidazole, un composé en forme d’anneau à base de nitrogène organique; les expériences ont démontré pour la première fois que les molécules d’eau peuvent être induites pour coller aux parois du canal, en vue de former un câble d’eau. Cornell dit que jusqu’à présent, les câbles d’eau ont été supposés mais n’ont jamais été vus.
‘J’appellerai cela la première véritable observation d’un câble d’eau.’ dit [Poul] Petersen. ‘Nous ne voyons pas que l’oxygène (les atomes), nous voyons les protons également. Il s’agit de la première observation de l’hydrogène se reliant à un câble d’eau.’
Une découverte clé de ce travail fut l’orientation dipolaire nette des molécules d’eau dans des canaux confinés qui a induit une polarisation spécifique du canal, et qui conduit le substrat à travers. La faculté de mimer cette action serait la norme d’or concernant une technologie de désalinisation, disent-ils. Mais cela est-il la manière dont les câbles d’eau fonctionnent dans les systèmes biologiques ?
Un aimant super puissant rencontre un câble d’eau biologique pour la première fois
Un des défis de l’observation les câbles d’eau biologiques est l’appairage à l’intérieur du confinement étroit d’un canal de la membrane. Un autre défi est le ralentissement de l’action. La formation du lien d’hydrogène est supposée changer des milliards de fois à la seconde. Cette année, une équipe internationale a utilisé l’ultra haute intensité d’un aimant dans le laboratoire du National High Magnetic Field lab à Tallahassee, en Floride, pour accomplir une avancée. En considérant que le champ d’énergie des machines d’IRM dans les hôpitaux marche aux alentours de 1 à 3 Teslas (T), le pouvoir de l’aimant à Tallahassee, 35.2 T, est vraiment incroyable. C’est un ordre de magnitude plus fort que le champ magnétique terrestre ou solaire.
Leur rapport dans PNAS, “Functional stability of water wire–carbonyl interactions in an ion channel,” (faculté fonctionnelle des câbles d’eau – interactions carbonyle dans un canal d’ion) raconte comment ils furent capables de réussir cet exploit dans un canal de membrane bien caractéristique appelé gramicidin A.
Les câbles d’eau sont cruciaux dans le fonctionnement de nombreuses membranes de protéines, comme dans les canaux qui conduisent l’eau, les protons, et d’autres ions. Ici, dans des couches doubles de lipide liquide et cristallin et sous des conditions environnementales symétriques, les interactions de liaison sélectives d’hydrogène entre huit eaux comprenant un câble d’eau et un sous ensemble d’oxygène carbonyle recouvrant le canal antiparallèle de gramicidin A dimérique sont caractérisées par une spectrométrie O NMR de 35.2 T par des études numériques.
Gramicidine A (gA), découvert en 1939, est un peptide antibiotique linéaire produit par le Bacillus brevis. Contrairement à la plupart des peptides, gA consiste en résidus d’amino-acides gauches et droits. Cela donne une forme hélicoïdale et en spiral qui pénètre la membrane de la bactérie, en formant un pore qui ressemble à un escalier en colimaçon. Cela permet le libre passage des cations (ions positivement chargés) afin de neutraliser le pH à l’intérieur et à l’extérieur. ‘L’activité antimicrobienne’, explique l’auteur, ‘dérive de sa capacité à former un canal transmembranaire qui est sélectif par rapport aux cations monovalents.’ (monovalent : en physique, désigne un atome qui ne peut présenter qu’une seule liaison avec un autre corps chimique; en biologie, qualifie un vaccin ou un sérum issu d’une seule souche microbienne et efficace uniquement sur cette souche.)
Il s’agit d’un canal simple à utiliser pour étudier l’activité d’un câble d’eau.
La colonne unique du pore aqueux, se terminant par les deux L10 carbonyles, est seulement assez large pour accueillir une colonne unique de molécules d’eau d’hydrogène lié : c’est-à-dire, un câble d’eau, de même pour des cations monovalents variés allant de Li+ to Cs+. Les plans de peptide de gA sont quasiment parallèles à l’axe du pore, avec des carbonyles impairs vers les surfaces double couche. En pénétrant la région du câble d’eau du canal, un cation interagit avec seulement deux eaux et forme une paire possible d’oxygène carbonyle en suivant une voie en spirale à travers le pore.
Une découverte surprenante fut que les liens d’hydrogène dans le câble sont beaucoup plus stables que prévu. Au lieu de changer en nanosecondes au sein du fort champ magnétique, ils s’attardent quelques millisecondes – six ordres de magnitude plus longs.
Les résultats révèlent que les oxygènes carbonyles sélectifs qui tapissent la paroi du pore forment des liens remarquablement stables avec le câble, à tel point que le câble d’eau ne change pas son orientation à l’échelle NMR de la milliseconde. L’orientation stable du dipôle du câble d’eau fournit aussi une explication simple pour la faible affinité sur le second site de liaison de cation dans ce canal dimérique, malgré une séparation de ∼24 Å à partir du premier site de liaison jusqu’à l’autre bout du pore.
Le dipôle formé par la différence de 24 fois dans les affinités de liaison force le cation à descendre dans le canal. Les molécules d’eau sont placées dans des positions précises pour fournir une stabilité optimale.
Le câble d’eau lui-même possède une échelle de stabilité allant du négatif du dipôle électrique vers le dipôle positif. Les interactions au bout de ce dipôle par rapport aux trois premières eaux du câble d’eau sont particulièrement stables.
Existe-il une raison pour laquelle les liens d’hydrogène ont besoin d’être stables ? Oui ; le temps de passage des cations requière que les sites de liaison ne s’inversent pas trop vite. Les câbles d’eau sont des assemblées biologiques critiques supportées par la membrane de protéines afin de transporter la charge et les ions à travers la membrane. Le caractère unique en haute résolution gA fournit des perspectives sur la dynamique, la structure et le mécanisme fonctionnel de ce canal d’ions.
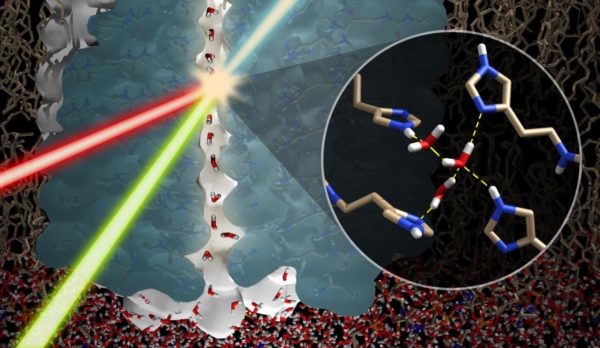
En résumé, l’écartement des acides aminés et des molécules d’eau est optimisé pour le fonctionnement. Le premier ion est aspiré, en formant son lien d’hydrogène avec l’eau, afin que le second ion entrant dans le canal n’inverse pas le dipôle et coupe le flux. Cela requière de la précision à la fois par rapport à la position et au temps. Il s’agit d’un des exemples les plus simples trouvés dans une bactérie. Il est juste de s’attendre à plus d’optimisation dans les futures études sur les câbles d’eau au sein de canaux de membranes plus complexes.
Est-ce que les auteurs pensent que cela est conçu de manière intelligente ? Ils disent presque cela :
L’influence profonde du canal d’eau dans ce modèle et l’eau stabilisée – les interactions carbonyles illustrent le sens et la fonctionnalité concernant de tels câbles dans de nombreux canaux et matériaux. En particulier, la stabilité du câble d’eau et de son dipôle électrique suggère que son influence dans de nombreux autres systèmes pourrait être plus significatif que généralement reconnue. Pour accomplir une telle compréhension, la spectroscopie O reportée ici, à la force de champ de 35.2 T démontre la sensibilité extrême à l’environnement chimique environnant les sites d’oxygène où beaucoup de la chimie biologique prend place.
Leur étonnement par rapport à ce système pourrait expliquer leur échec à l’attribuer à l’évolution.
ST, cycle de Vajrayogini 2020, Provence
Source :







Laisser un commentaire